目前,伴隨診斷在腫瘤學中大量應用,在為腫瘤患者爭取寶貴時間和節省不必要費用的同時,也為藥企細分市場促進研發提供了依據。與此同時, 伴隨診斷也逐步進入其他疾病類別藥品的研發中,逐步成為加速新藥審批的利器。因此,大量的研發力量和資本被投入到發現、確認以及推廣伴隨診斷和伴隨生物標記物中來。
在商業領域,以伴隨診斷為核心的戰略合作和收購也不斷涌現。可以預見,伴隨診斷將持續地為病人,醫生,藥企,以及政府監管方提供極具價值的可靠信息,將進一步推進精準治療的完善。
筆者希望通過此文,讓伴隨診斷為更多的大眾和投資者了解和熟悉。
這篇文章分成三個部分:
第一, 簡要介紹伴隨診斷;
第二,討論伴隨診斷的發展現狀和未來的發展趨勢,著重探討伴隨診斷在腫瘤癌癥方面和新藥審批方面的應用;
第三,聚焦伴隨診斷的商業機會,梳理以其為核心的研發和商業交易。

疾病診斷醫治的變遷
伴隨診斷簡介
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">什么是伴隨診斷?
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">根據美國食品藥品管理局(Food and Drug Adminstration, FDA),伴隨診斷一般是指內用的醫療儀器或測試方式,為相應藥物的安全性和有效性提供極具價值的信息。依據伴隨診斷結果,醫生可以更加準確地判斷,針對這種藥物或者療法,
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">1. 哪一類病人最可能受益;
portant; word-wrap: break-word !important;">2. 哪一類病人最可能有更高的風險;
portant; word-wrap: break-word !important;">3. 觀察療效調整治療方案以期提高療效和安全性。 一套完善可靠的伴隨診斷體系對藥物的經濟有效安全使用至關重要。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">從歷史的角度來看,最早的伴隨診斷出現在20世紀80年代。當初,藥企對這種將細分市場的診斷心存疑慮,因為推出伴隨診斷就意味著某種藥品的使用病人減少了。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">然而伴隨診斷在羅氏公司(Roche)生產的治療乳腺癌的Herceptin®(赫賽汀) (通用名:trastuzumab, 曲妥珠單抗) 和諾華公司(Novartis)生產的治療白血病的Gleevec®(格列衛)(通用名:imatinib,伊馬替尼) 兩種藥的商業成功后,這個領域逐步發展起來。從最早只是抗腫瘤藥到現在各大疾病領域,伴隨診斷數目增至最初的12倍。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">截至2012年,伴隨診斷及其藥物有多達63種,主要集中在抗腫瘤和免疫調節,心血管和抗感染。其中,抗腫瘤藥物有超過40%的市場份額。不難想象,抗腫瘤藥物的伴隨診斷仍是主要力量。雖然藥物的適用病人數量減少,但由于可以相對定高價,所以可以取得與傳統上暢銷藥一樣取得年收入超過10億美元。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">在目前討論很火熱的腫瘤免疫療法來看,伴隨診斷與之有很大的關聯。在PD-1類的抗癌藥中,Bristol-Myers Squibb (BMS)公司生產的Opdivo®(Nivolumab)直接作用于PD-1,是目前賣的最好的PD-1藥。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">有趣的是,BMS號稱這款藥不需要對病人PD-1水平進行測試。默沙東/默克公司(Merck)的Keytruda®(Pembrolizumab)同樣是直接作用于PD-1的但在其說明書上指明需要伴隨診斷結果是PD-L1高表達的病人。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">還有一種是由羅氏公司(Roche)旗下的基因泰克公司(Genentech)研發的Tecentriq®(Atezolizumab),這藥作用于PD-L1。對伴隨診斷的態度處于上面兩種藥之間,說明書中沒有要求必須要有伴隨診斷結果,但指出有較高PD-L1水平的病人會有三倍以上的有效性。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">今年大熱的另一種免疫療法CAR-T也預計會有伴隨診斷地大量參與。今年,美國FDA批準了諾華生產的治療25歲以下復發性的B細胞急性淋巴性白血病的Kymriah,和Gilead/Kite生產的治療成人復發性B細胞淋巴癌的Yescarta。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">目前,免疫療法的應用都在血液腫瘤領域,實體瘤還需進一步研究。另一方面,免疫療法的副作用和安全性也令人關注。部分在研藥物出現病人死亡而被叫停。上述兩款藥雖然暫時都沒有伴隨診斷問世,但預計隨著人們對藥物副作用和病人情況的認識的加深,伴隨診斷很可能會推出。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">中國創新藥在腫瘤免疫療法,特別是CAR-T這個新領域發展勢頭很好。以CAR-T登記的臨床試驗數量大大超過美國。所以中國的藥企可以加大對伴隨診斷的研究來取得這個領域的優勢。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">在抗腫瘤藥物之外的其他疾病領域,伴隨診斷也大顯身手。比如囊性纖維化(cyclic fibrosis),艾滋病 (HIV),和嚴重發育障礙。下面舉幾個例子:
portant; word-wrap: break-word !important;">
- portant; word-wrap: break-word !important;">
-
由Vertex Pharmaceuticals公司生產的治療囊性纖維化的Kalydeco®(ivacaftor)是基于CFTR基因的G551D突變。目前FDA批準了Luminex的xTAG Cystic Fibrosis 60 Kit v2 測試和TM Bioscience的Tag-It Cystic Fibrosis Kit用于測試這種基因突變。據預計,Kalydeco®將在2018年有超過20億美元的銷售額。
portant; word-wrap: break-word !important;">
- portant; word-wrap: break-word !important;">
-
用于治療HIV病人的Selzentry® (maraviroc) 的作用機制是藥物結合正常巨噬細胞和T細胞表面的CCR5受體,從而阻斷HIV病毒進入這些細胞。因為HIV還可能通過其他細胞表面受體,所以要篩選有盡可能少其他受體的病人進行這種藥物的治療。具體是用由Monogram Biosciences 公司(現在屬于LabCorp公司)研發的Trofile®, 一種HIV coreceptor tropism測試。
portant; word-wrap: break-word !important;">
- portant; word-wrap: break-word !important;">
-
在治療嚴重發育障礙的病人時常用Increlex® (mecasermin),在治療時需要測試 病人體內IGF-1 (insulin-like growth factor 1)的含量。
portant; word-wrap: break-word !important;">
伴隨診斷發展現狀和未來趨勢
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">目前,據clinicaltrials.gov網站報道,大約100種在臨床II,III,IV期的藥物附有診斷相關信息,包括主要和次要結果指標檢測(primary and secondary outcome measures),和病人有效性 (inclusion/exclusion eligibility criteria)。雖然不是每一個臨床試驗藥物都能成功獲批上市,但是這表明可能有100種伴隨診斷的測試或儀器有市場機會。畢竟,伴隨診斷的結果能讓藥企明確最能受益的病人;或者,相反地,知道哪一類病人有更大的風險或無作用。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">美國FDA鼓勵支持伴隨診斷的研發。早在2004年FDA發布的關鍵渠道研發的白皮書里就有相關闡述。目前有4種藥必須要有伴隨診斷結果之后才有使用。在國際范圍內,歐洲藥品管理局(European Medicines Agency, EMA)有相似的情況,也需要待批藥品有相關的診斷測試。兩個機構對具體藥物的要求稍有不同。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">在美國FDA,歐洲EMA,和日本藥監局之間,目前有一個非盈利性組織Critical Path Institute (C-Path)來協調藥物研發合作,這樣藥企就可以放心地分享可能是商業秘密的數據資料。這個機構一個很重要的目的就是加強伴隨診斷的合作。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">雖然目前藥品和相關伴隨診斷在時間上并沒有同步 — 據統計,只有11%的要求有伴隨診斷的藥品是和其伴隨診斷同時獲批的,而大部分的伴隨診斷是在某種藥品已經上市,然后其伴隨診斷才被FDA批準 — 但是隨著越來越多的藥品臨床試驗利用伴隨診斷去選擇病人樣本,藥品及其伴隨診斷同時獲批將會越來越普遍。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">在具體市場預測方面,縱觀全球,伴隨診斷市場在2016年達到44億美元(約合290億人民幣)。據BCC Research預測,這個市場將在2022年增至251億美元(約合1650億人民幣),復合年增長率高達35.5%。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">2017年標示著伴隨診斷進入新的時期。5月末,FDA批準默克/默沙東(Merck/MSD)的checkpoint inhibitor, Keytruda。這是首次FDA批準了基于基因指紋而不是腫瘤來源器官的抗腫瘤藥物。當然,我們也要看到批準到大量應用的障礙,比如采集基因指紋需要腫瘤病人對他們的腫瘤進行基因測序,另外,在目前的醫療體系中,腫瘤科醫生往往是在某一類器官的腫瘤專家。而目前研究表明腫瘤發生非常復雜,具有異質性(heterogeneity)。這就導致某些乳腺癌的癥狀和治療方法更像皮膚癌。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">另一個突破是FDA批準(premarket approval)了一款針對多個藥物的伴隨診斷,oncomine Dx Target Test。這個測試是由賽默飛公司(Thermo Fisher Scientific)研發,運用下一代測序技術來篩查23個癌癥基因。該公司表示他們將繼續研發,把更多的癌癥基因納入他們的診斷測試中。在目前被批準的23個基因中,有三個基因可以成為治療非小細胞肺癌的三種不同療法的伴隨診斷。這種一石多鳥的策略為癌癥病人,特別是病情復雜的患者,提供了快速經濟的診斷途徑。
portant; word-wrap: break-word !important;">
伴隨診斷發展現狀和未來趨勢
portant; word-wrap: break-word !important;">
伴隨診斷的商業交易
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">對一個行業或市場的活躍程度的判斷,商業交易是一個很好的參照。近些年來與伴隨診斷相關的商業交易逐步增多。雖然在所有診斷相關交易中,伴隨診斷仍然只占個位數的比例;但三年來,這個比例已增至12%。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">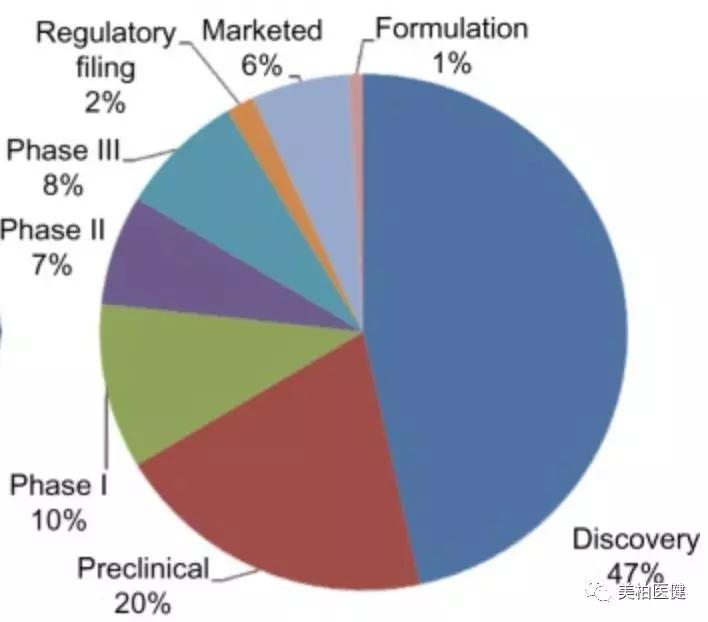
portant; word-wrap: break-word !important;">伴隨診斷的商業交易類別(adapted from Agarwal et al.,2015)
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">如果我們聚焦在商業交易的種類上,可以發現大部分公開的交易都是處于藥物探索階段,疾病領域也是主要在抗腫瘤藥物方面。具體說來,在研發前期的合作協議中,伴隨診斷的研發方往往希望收取藥品獲批成功上市后銷售額的一定比例,當然他們也共同承擔著藥品失敗的風險。例如,在2012年1月,羅氏基因泰克公司(Roche/Genentech)和Xenon Pharmaceuticals簽署了高達6.46億美元的治療緩解疼痛的化合物和伴隨診斷的合作研發協議。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">從商業交易的角度來看,伴隨診斷的市場價值從研發到后期上市逐步減少。特別是當藥物已經成功上市以后再推出的伴隨診斷。比如,對年收入超過10億美元的blockbuster藥,其后推出的伴隨診斷很少超過1億美元。這種現象背后的一個重要原因就是診斷方法或儀器很少擁有和藥物本身一樣的知識產權保護;而一種藥往往有幾個FDA批準的伴隨診斷。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">近幾年的一個新趨勢是,更多的藥企愿意先期贊助伴隨診斷研發方。這種現象尤其在醫療服務由政府買單的歐洲國家比較多見。一部分的原因是在實際的操作中,還需要考慮花費在向醫護人員宣傳推廣伴隨診斷方式,保證有可靠的測試實驗室,已經能從醫療保險方取得保險報銷。近些年來比較活躍的大型藥企包括羅氏(Roche),輝瑞(Pfizer), 默克/默沙東(Merck, MSD), 阿斯利康(Astra Zeneca), BMS (Bristol Myers Squibb), 安進(Amgen), Biogen, 和禮來(Eli Lilly)。
portant; word-wrap: break-word !important;">
研發伴隨診斷的商業路徑
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">從商業戰略上講,對于想要研發伴隨診斷的藥企來說,主要有三條途徑可以達到目的。第一是內部研發,第二是與一家成熟的診斷公司合作,第三是并購一家診斷公司。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">第一條路需要藥企自己有一套相對成熟的伴隨診斷研發體系,比如羅氏(Roche)旗下的Roche Diagnostics。他們有幾個成熟的診斷研發平臺,包括分子診斷 (Roche Molecular平臺),生理病理學(Ventana Medical Systems平臺),免疫學(Roche Professional平臺)。之前,Novartis和Abbott也有相關的部門,直到前段時間 Novartis Diagnostics和 Abbvie分別從兩家分離開來。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">第二條路需要和成熟的診斷公司合作。這些診斷公司包括Agilent-Dako, Thermo Fisher-Life Technologies, Labcorp-Genzyme Genetics, 和Qiagen-DxS。 由于它們的影響力,這些企業往往能在與藥企合作中有很大的話語權。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">最后一個選項是藥企收購一個診斷研發企業從而快速建立伴隨診斷的研發能力。比如,2010年,禮來(Eli Lilly)花3億美金收購了Avid Radiopharmaceuticals,正是看中了它在阿爾茲海默癥診斷領域的實力。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">建立伴隨診斷研發能力的三種途徑
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">
結語
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">未來的醫療診斷和治療將是在個體化水平進行醫治,針對每個病人不同的情況推薦不同的藥物和計量。可以說,個體化醫藥和精確治療的宗旨就是選擇合適的劑量的合適的藥品,在合適的時間,用于合適的病人。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">這就需要我們能相對精確地測試病人群體的相似性和差異性,基于這些測試結果給出不同的治療方案。這些協同藥物的測試診斷,從廣義上來講,就是藥物的伴隨診斷。不難想象,伴隨診斷就是通往未來醫療的一把金鑰匙。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">伴隨診斷未來大有所為,市場發展空間巨大。未來伴隨診斷的發展將受益于一個更加有生機的生態系統,包括大型制藥企業持續地支持生物標記物的探索,診斷企業不斷創新研發更有效的測試,政府監管部門加快同步批準藥品和其伴隨診斷,最后還有醫療保險公司充分識別涵蓋伴隨診斷所帶來的經濟效益。
portant; word-wrap: break-word !important;">
portant; word-wrap: break-word !important;">當然充足的資本也是必不可少的。除了傳統的企業融資手段,風險投資也逐步顯現出巨大作用。比如,2013年的統計顯示,分別有2億9千萬和4億5千萬美金來自早期和晚期的風險投資,其他的大約10億美金來自企業債,IPO,IPO增發,和并購交易。





